مهندسی شیمی
دانلود جزوه -کتاب-مقالهمهندسی شیمی
دانلود جزوه -کتاب-مقالهاندازه گیری قلیائیت آب
اندازه گیری قلیائیت آب
قلیائیت به صورت P Alk یا M Alk (یا T Alk) نشان داده می شود و برحسب ppm CaCO3 گزارش می شود.
منشاء قلیائیت در آب وجود یون های هیدروکسید (-OH) ، کربنات (2-CO3) و بی کربنات (-HCO3) می باشد. البته براتها (3-BO3) ، فسفات ها (3-PO4) و سیلیکات ها (3-SiO3) نیز می توانند ایجاد قلیائیت کنند.
قلیائیت آب ، ظرفیت کمی آب در خنثی نمودن یک اسید قوی تا PH مورد نظر می باشد. تعیین قلیائیت در تفسیر و کنترل فرآیندهای تصفیه آب و فاضلابها کاربرد فراوانی دارد.
قلیائیت می تواند به پنج صورت زیر وجود داشته باشد:
- محلول فقط شامل هیدروکسید (-OH) باشد.
- محلول فقط شامل کربنات (2-CO3) باشد.
- محلول فقط شامل بی کربنات(-HCO3) باشد.
- محلول شامل کربنات و بی کربنات (2-CO3) و (-HCO3) باشد.
- محلول شامل هیدروکسید و کربنات (-OH) و (2-CO3) باشد.
در صورتی آب دارای قلیائیت است که PH آن از 4.6-4.3 بالاتر باشد.
قلیائیت شامل قلیائیت فنل فتالئین (P) و متیل اورانژ یا قلیائیت کل (T یا M) می باشد.
قلیائیت فنل فتالئین مربوط به نمکهائی است که PH آنها از 8.2 (PH تغییر رنگ فنل فتالئین) بالاتر باشد یعنی نمکهایی است که دارای عامل هیدروکسید(-OH) و کربنات (2-CO3) هستند.
قلیائیت متیل اورانژ شامل قلیائی هایی است که PH آنها از 4.5 (PH تغییر رنگ متیل اورانژ) بالاتر باشد یعنی قلیائی هایی که شامل هیدروکسید (-OH) ، کربنات (2-CO3) و بی کربنات (-HCO3) هستند.
برای اندازه گیری قلیائیت از یک اسید قوی مانند اسید سولفوریک یا اسید کلریدریک 0.02 نرمال استفاده می کنند.
روش تعیین قلیائیت
به حجم مشخصی از نمونه چند قطره معرف فنل فتالئین اضافه می کنند (حجم بستگی به قلیائیت نمونه دارد) اگر قلیائیت بالا باشد حجم کمتری انتخاب می کنیم اگر محلول تغییر رنگ نداد محلول قلیائیت فنل فتالئین ندارد (PH=0) و حاوی یونهای هیدروکسید و کربنات نیست اگر بعد از اضافه کردن فنل فتالئین رنگ محلول ارغوانی شد محلول دارای قلیائیت فنل فتالئین است. سپس محلول را با اسید کلریدریک 0.02 نرمال تیتر می کنند تا محلول بی رنگ شود. حجم اسید کلریدریک مصرفی را یادداشت می کنند. (A cc)
برای تعیین قلیائیت متیل اورانژ چند قطره معرف متیل اورانژ اضافه کرده و در صورتیکه رنگ محلول قرمز مایل به پوست پیازی شد نشان دهنده P=M است. اگر رنگ محلول زرد شد عمل تیتراسیون با اسید کلریدریک 0.02 نرمال را ادامه داده تا رنگ محلول به نارنجی یا پوست پیازی تغییر رنگ دهد. حجم اسید مصرفی را یادداشت می کنند. (B cc)
چنانچه تشخیص نقطه پایان تیتراسیون در قلیائیت متیل اورانژ مشکل باشد از PH متر یا معرف مخلوط استفاده می کنند. معرف مخلوط (Indicator Mix) مخلوط دو معرف متیل رد و برموکروزول می باشد و تغییر رنگ از سبز به صورتی می باشد.
مراحل ختم عمل در Indicator Mix:
| آبی – سبز |
PH > 5.2 |
| سبز | PH = 5 |
| صورتی – خاکستری | PH = 4.8 |
| صورتی | PH = 4.6 |
نقطه پایان تیتراسیون در PH = 4.6 و تغییر رنگ از سبز به صورتی می باشد.
چگونگی ایجاد قلیائیت در آب
اسیدیته و قلیائیت آب ، هر دو به مقدار CO2 محلول در آب بستگی دارند. CO2 در آب حل شده و اسید کربنیک تولید میکند. اسید حاصله در داخل آب ، یونیزه شده و پروتون و یون بیکربنات ایجاد میکند. پروتون با کربنات کلسیم ترکیب شده و با تولید بیکربنات باعث تبدیل کربناتها به بیکربنات میشود و در نتیجه حلالیت کربنات کلسیم در آب افزایش مییابد.شکلهای گوناگون CO2 محلول در آب در PH های مختلف
CO2محلول در آب در PH کمتر از 4 به صورت اسید کربنیک میباشد. با افزایش PH ، اسید کربنیک به بیکربنات تجزیه میشود. در 6.3=PH مقدار اسید کربنیک و بیکربنات در آب با هم برابر میباشد. در 8.3 = PH ، فقط بیکربنات وجود دارد و با افزایش مجدد PH مقدار کربنات در محلول بیشتر میشود، بطوری که در 10.3= PH مقدار کربنات و بیکربنات باهم برابرند. در 11.3 < PH فقط کربنات در محیط وجود دارد.قلیائیت کل آب
قلیائیت کل آب شامل رادیکالهای هیدروکسید ، کربناتها و بیکربناتها و در برخی مواقع شامل فسفاتها ، بوراتها و سیلیکاتها میباشد. قلیائیت هیدروکسید شامل میباشد و مهمترین کربناتهای آب عبارتند از
میباشد و مهمترین کربناتهای آب عبارتند از  بیکربناتهای مهمی که معمولا در آب وجود دارند عبارتند از
بیکربناتهای مهمی که معمولا در آب وجود دارند عبارتند از 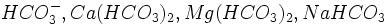 .
. شناساگر مورد استفاده
شناساگرهای مورد استفاده در تعیین قلیائیت آب عبارتند از فنل فتالین و متیل اورانژ. تیتراسیون معمولا یک اسید قوی استاندارد نظیر اسید سولفوریک و اسید کلریدریک انجام میشود. در تیتراسیون با فنل فتالین ، اگر رنگ شناساگر که در داخل محلول نمونه بعلت محیط قلیائی ارغوانی باشد و در 8.3=PH بیرنگ شود، مقدار اسید مصرفی خنثیسازی قلیائیت ناشی از هیدروکسید و کربنات را نشان میدهد.اگر به این نمونه چند قطره متیل اورانژ اضافه شود، رنگ محیط نارنجی زرد خواهد شد که با تیتراسیون توسط اسید در 4.5= PH رنگ محلول سرخ خواهد شد. این مقدار اسید در واقع برای خنثی سازی بیکربناتها بکار رفته است. مجموع قلیائیتهای فنل فتالین و متیل اورانژ را قلیائیت کل مینامند و با علامت اختصاری T نشان میدهند.
T = P + M
در رابطه مقابل ، M ، بیانگر اسید مصرفی برای خنثی کردن بیکربناتها ، P ، اسید مصرفی برای خنثی کردن هیدروکسید و کربنات و T ، قلیائیت کل است.
حالتهای مختلف قلیائیت آب
- اگر P=T پس M=0 یعنی در محیط کربنات و بیکربنات وجود ندارد و قلیائیت مربوط به هیدروکسیدهاست.
- اگر
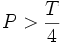 قلیائیت مربوط به هیدروکسیدها و کربناتها میباشد.
قلیائیت مربوط به هیدروکسیدها و کربناتها میباشد.
- اگر P = M پس
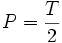 قلیائیت مربوط به کربناتها میباشد.
قلیائیت مربوط به کربناتها میباشد.
- اگر
 قلیائیت مربوط به کربناتها و بی کربناتها میباشد.
قلیائیت مربوط به کربناتها و بی کربناتها میباشد.
- اگر P = 0 قلیائیت مربوط به بیکربناتها میشود. دراین صورت 8.3 > PH بوده و T= M خواهد بود.
نکته مهم
در محیط بازی که یونهای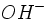 وجود دارند، بیکربناتها وجود ندارند و عموما به کربنات تبدیل شدهاند. از
آن رو درصورت موجود بودن قلیائیت هیدروکسید ، مقدار قلیائیت بیکربنات
عملا صفر خواهد بود. البته عکس این مطلب هم صادق است.
وجود دارند، بیکربناتها وجود ندارند و عموما به کربنات تبدیل شدهاند. از
آن رو درصورت موجود بودن قلیائیت هیدروکسید ، مقدار قلیائیت بیکربنات
عملا صفر خواهد بود. البته عکس این مطلب هم صادق است.